Az anyagok különféle halmazállapotai
A különféle időjárási jelenségek kapcsán gyakran találkozunk az anyagok halmazállapot-változásával. Ott van máris a víz, amelyből egy nagyobb lehűlés során jég lesz, erősebb felmelegedés hatására viszont párologni kezd, vagyis gőzzé válik. Sőt, ha a levegőben lévő pára a levegőnél hűvösebb hőmérsékletű fűszálra hullik, akkor ismét apró vízcseppekké válik, vagyis lecsapódik a füvön harmat vagy dér formájában.
Szilárd, folyékony, gáz és plazma
Négyféle halmazállapot létezik: szilárd, folyékony, gáz (más szóval: gáznemű, illetve gőz) és plazma állapot. A plazma és a szilárd halmazállapotot gyűjtőnéven kondenzált (sűrített) halmazállapotnak nevezik, a légnemű és folyékony halmazállapotú anyagok gyűjtőneve pedig cseppfolyós közeg, vagy csak közeg. A folyadékok jellemzően abban különböznek légnemű halmazállapotú anyagoktól, hogy azokkal ellentétben szabad felszínnel rendelkeznek.
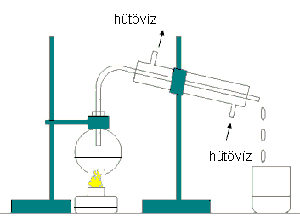 |
| Az egyszerű desztillációs készülékek szerkezete. Az ennél összetettebb módszerekről itt olvashatsz. (Kép forrása: vilaglex.hu) |
Elméletileg minden anyag mind a négy halmazállapotban előfordulhat, a gyakorlatban azonban több olyan szilárd anyag is létezik, amely már az olvadáspontjánál alacsonyabb hőmérsékleten elbomlik vagy átalakul, és így nem éri el a folyékony állapotot. Ezek olvadáspontját inkongruens (magyarul „nem egyező”, „nem egybevágó”) olvadáspontnak nevezik.
Az olvadáspont az a hőmérsékleti szint, amelyben egy anyag éppen egyensúlyban van a szilárd halmazállapotból a folyadék halmazállapotba való átmenet során. Például a jég olvadáspontja közismerten 0 °C. De például a nádcukoré 160 °C (vagyis ezt csak folyamatosan hevített lábosban tudjuk elfolyósítani), az alumíniumé 660 °C, az ezüsté 960,8 °C, a higanyé viszont kiemelkedően alacsony: ez a fém már –38,36 °C-on felolvad és folyékonnyá válik, ha addig fagyott állapotban volt.
Az olvadáspont ellenpárja a fagyáspont (ezt más néven dermedéspontnak is hívják), amely számszerűen ugyanaz a hőmérsékleti érték, mint az olvadáspont, csak ilyenkor a másik irányból – vagyis a folyékonyból a szilárdba irányuló folyamat felől – határozzuk meg. A víznek tehát a fagyáspontja és az olvadáspontja egyaránt 0 °C, vagyis például egy tó ugyanúgy nulla foknál fagy be, ahogyan annál is olvad fel a jege.
Az olvadás és a fagyás a tiszta anyagok esetében izoterm folyamat, ami arra utal, hogy az anyagon belül egyenlő a hőmérsékleti eloszlás. (A szó az „egyenlő” jelentésű, görög „iszosz” szóból ered, amellyel még az „izocukor” vagy az „izotóp” szóban is találkozhatunk.)
Érdekes jelenség, hogy a szilárd anyagoktól eltérően a folyadékok nem feltétlenül fagynak meg az egyensúlyi fagyásponton, ezért túlhűthetők.
A tiszta szilárd anyagok olvadáspontja nemcsak a hőmérséklettől, hanem a nyomástól is függ. Általánosságban a nyomás növekedésével az olvadáspont szintje is növekszik, ami alól azonban vannak kivételek. Ilyen például a jég és a bizmut, amelynél ez fordítva történik.
Mindezek mellett vannak olyan anyagok is, amelyek már a forráspontjuknál alacsonyabb hőmérsékleten elbomlanak, és így ezeknek nem létezik légnemű halmazállapotuk. Ez azonban már a „forráspont” fogalmával függ össze.
A forráspont és a párolgás
Forráspontnak azt a hőmérsékletet nevezzük, amelynél a gőz nyomása egyenlő a külső nyomással (vagyis a levegő nyomásával). Ebből következően a víz forráspontja csak a tengerszint magasságában, 1 atm nyomáson 100 °C, nagyobb nyomáson (például a kuktafazékban) magasabb, kisebb nyomáson (például magasabb hegyeken) alacsonyabb hőmérsékleten forr fel a víz. Ha a víz 1 atmoszféra nyomáson nem 100 °C-on forr fel, az azt jelzi, hogy nem tiszta. A víz a forrásától kezdve válik fokozatosan gőzzé, amely abban az esetben alakul vissza vízzé, ha hidegebb felülettel érintkezik. Ilyenkor cseppenként lecsapódik, aminek a jelenségével szintén gyakran találkozunk a természetben. A pára lecsapódását jelenti például a hajnali harmat a füvön, vagy a dér a fák ágain. Amikor jégkristályok csapódnak le az ágak szélfútta részein, olyankor zúzmara keletkezik.
 |
| A természet egyik legérdekesebb jelensége a zúzmarásodás. A zúzmara jégkristályokból áll, és a 0° C alá hűlt felületeken keletkezik, a tárgyak szélfútta oldalán. A lerakódás gyakran olyan, mintha madártollak nőttek volna például egy faágon. (Fotó: Craig Thom, South Africa, Wikimedia) |
A víz lecsapódási képességét egyébként kiválóan fel lehet használni arra, hogy minden fölösleges anyagtól mentes, tökéletesen tiszta vizet nyerjünk, amelyet a gyógyászatban lehet jól hasznosítani. Ez a desztillált víz, amelyet úgy állítanak elő, hogy felforralják a vizet, majd az abból keletkező gőzt hűtött csövön vezetik el. A gőz a hőkülönbség miatt lecsapódik a csőben, majd a végén egy másik edénybe csöpög. És mivel a vízben oldott, egyéb anyagoknak magasabb a forráspontjuk, azok a 100 °C-on nem forrnak fel, ezért már a gőzbe sem kerülnek bele, így végül a másik edénybe biztosan tiszta víz kerül.
A halmazállapotok „királynője”: a plazma
A „plazma” eredetileg azt jelentette, hogy „formázott, gyúrt anyag” (a görög „plaszma” alapján). A szót kezdetben csak a vérplazmára, vagyis a vér halványsárga folyadék-összetevőjére használták. Attól kezdve azonban, hogy felfedezték az ionizáció jelenségét, a kifejezést arra használjuk, amikor az anyagot alkotó atomokról egy vagy több elektron leszakad, és így az anyag az ionok és a szabad elektronok keverékévé válik. Vagyis az ionizált gázok neve lett a plazma. Ez egyébként a világegyetemben csupán igen magas hőmérsékleten, tízezer kelvin körül lehetséges, mert csak itt van jelen az elektronok leszakításához szükséges energia. Mivel az elektronok ettől kezdve már nincsenek az atomokhoz kötve, hanem szabadon mozoghatnak, a plazma elektromosan vezetővé válik és kölcsönhatásba lép az elektromágneses mezőkkel.
Bármennyire is hihetetlen: a világegyetem leggyakoribb anyaga a plazma. A csillagok is plazmaállapotú anyagból állnak (ezért lövellik ki magukból az ún. napszelet, amely valójában egy nagyobb, összeállt plazmatömeg), de a csillagközi térben is sok a plazma. Ám mivel a csillagközi tér nagyon tág és a plazmák minden helyet igyekeznek betölteni, a sűrűségük nem túl nagy, ezért az ilyen fajta plazmát "híg plazmának" is szokták nevezni.
Plazmaállapot a Földön is keletkezhet, például gyors égéskor, de a villámlásnál is létrejön plazma. Egyszerű plazmát szobahőmérsékleten is elő lehet állítani, nagy nyomással. Ez a hideg plazma, amely akkor keletkezik, ha két elektróda közé hélium és oxigén keverékét juttatjuk be.
A kifejezéssel a hétköznapi életben a leggyakrabban a plazmatévék kapcsán találkozhatunk. Ezek képcsöveit egy Angliába emigrált, Nobel-díjas magyar tudós, Gábor Dénes kutatásainak köszönhetjük. A plazmatévéknél olyan képcsöveket használnak, amelyekben a neon és xenon gázok keverékében jön létre az ionizáció. A folyamatot nagy UV-sugárzású kisülés kíséri, és ez készteti a képpont anyagát a színes fény sugárzására. A plazmatévék nagy előnye, hogy mivel minden egyes képpont egymástól függetlenül, akár folyamatos üzemben vezérelhető, a monitor mentes a szemnek ártó kellemetlen villogástól.
Lévai Júlia


